Umstellung von quadrivalenter auf trivalenter Version entsprechend der WHO-Empfehlung erfolgt bei gleichbleibendem Wirksamkeitsprofil sowie Verträglichkeit
Bad Homburg v. d. Höhe, 07. Januar 2025 — Das Gesundheitsunternehmen Viatris gibt bekannt, dass es die Zulassungen für seine Influenzaimpfstoffe Influvac®1 und Xanaflu®2 in Deutschland – neben 17 anderen europäischen Ländern – als trivalente Version für die nächste Grippesaison 2025/2026 erhalten hat. Dies entspricht den Empfehlungen der Weltgesundheitsorganisation3 (WHO) und der Europäischen Arzneimittelagentur4 (EMA), die einen Wechsel von quadrivalente auf trivalente Influenzaimpfstoffe gefordert hatten. Die Ständige Impfkommission5 (STIKO) hatte ihre Influenza-Impfempfehlung daraufhin angepasst.
Die EMA aktualisiert jährlich die Impfstoffempfehlungen für Europa, da sich die Influenzaviren ständig weiterentwickeln. Als Grundlage dienen Beobachtungen der WHO über die Prävalenz und die Merkmale der weltweit zirkulierenden Virusstämme. Seit der Impfsaison 2018/2019 enthielten die Influenzaimpfstoffe zwei Influenza-A-Stämme und zwei Influenza-B-Stämme – A(H1N1), A(H3N2), B/Victoria-Stamm und B/Yamagata-Stamm. Der B/Yamagata-Stamm wurde allerdings seit März 2020 nicht mehr in zirkulierenden Influenzastämmen nachgewiesen, was als epidemiologischer Erfolg zu werten ist, da seine Aufnahme nicht mehr erforderlich ist3 (siehe primäre Abbildung/Abbildung 1). Wichtig zu betonen ist, dass das Wirksamkeitsprofil und die Verträglichkeit bei dem trivalenten Impfstoff gleichbleibend gegenüber der bisherigen quadrivalenten Version ist.
Viatris ist der WHO-Empfehlung zur Umstellung von quadrivalente auf trivalente Influenzaimpfstoffe gefolgt und hat mit dem Vorlauf zur Produktion seiner trivalenten Influenzaimpfstoffe Influvac und Xanaflu für die Saison 2025/2026 begonnen (aktuell noch als quadrivalente Influenzaimpfstoffe Influvac Tetra6 und Xanaflu Tetra7 erhältlich).
Ergänzend in der Fachinformation der trivalenten Impfstoffe Influvac und Xanaflu steht die Information zu schwangeren Frauen „Influvac/Xanaflu wird angewendet bei Erwachsenen, einschließlich schwangeren Frauen, und bei Kindern ab 6 Monaten“ nun auch in der Kategorie „4.1 Anwendungsgebiete“.
Die Influenza stellt nach wie vor eine nicht zu unterschätzende Herausforderung für die öffentliche Gesundheit in ganz Europa dar8. Auf Deutschland bezogen wurden in der Grippesaison 2023/2024, einer eher durchschnittlich verlaufenden Grippesaison, 211.000 Fälle registriert9. Man geht allerdings davon aus, dass in Deutschland noch deutlich mehr Menschen erkrankt waren, da nicht alle Fälle erfasst wurden. 10.290 der erfassten Grippe-Fälle führten in der Grippesaison 2023/2024 in Deutschland zu Krankenhausaufenthalten und 1.119 zum Tod10. Darüber hinaus verursacht die Influenza erhebliche wirtschaftliche Kosten, einschließlich Produktivitätsverlusten und Fehlzeiten11. Wichtig ist, in diesem Zusammenhang zu berücksichtigen, dass jede Influenzasaison individuell verläuft.
Trotz der Verfügbarkeit wirksamer Impfstoffe wurde in vielen Regionen Europas das von der WHO empfohlene Impfziel von 75 Prozent für Risikogruppen nicht erreicht. Auch Deutschland ist gerade in Bezug auf die Chroniker unter 60 Jahren mit 23,4 Prozent von diesem Ziel weit entfernt12. Die letzte Grippesaison war besonders signifikant, vor allem für gefährdete Bevölkerungsgruppen wie ältere Erwachsene und Kleinkinder, wobei die höchste Aktivität Anfang 2024 auftrat13. Dies deutet darauf hin, dass eine Erhöhung der Durchimpfungsrate von entscheidender Bedeutung ist, um die Auswirkungen der Grippe abzumildern, da die Immunisierung nach wie vor die wirksamste Maßnahme zum Schutz vor dem Virus ist14. Es ist nie zu spät, sich gegen die Grippe impfen zu lassen und sich und seine Mitmenschen zu schützen. Für eine Immunisierung, auch noch zu Beginn des Jahres 2025, stellt Viatris weitere Impfdosen zur Verfügung. Influvac Tetra und Xanaflu Tetra können kurzfristig über die bekannten Kanäle bezogen werden.
Die Influenzaimpfstoffe von Viatris, die bereits seit 1950 verwendet werden, haben ein bewährtes Sicherheitsprofil und wurden weltweit mehr als 800 Millionen Mal verabreicht15. Viatris hat bedeutende Erfahrungen im Zusammenhang mit saisonalen Influenzaimpfstoffen – ob trivalent oder quadrivalent – gesammelt und feiert dieses Jahr bereits den 75. Jahrestag seines Grippeimpfstoffs Influvac. Das positive Nutzen-Risiko-Profil von Viatris‘ Influenzaimpfstoff Influvac wurde für alle Bevölkerungsgruppen ab sechs Monaten nachgewiesen, auch für Personen mit Grunderkrankungen und Schwangere. Dies wird durch über 40 Jahre veröffentlichte klinische Daten aus 89 klinischen Studien sowie durch regelmäßige Sicherheitsbewertungen nach der Markteinführung gestützt.15-17
„Die Empfehlungen der WHO und der EMA haben für uns die höchste Priorität, um die höchsten Standards für Qualität unserer Influenzaimpfstoffe einzuhalten. Unsere langjährige Erfahrung und klinische Daten belegen das bewährte Sicherheits- und Wirksamkeitsprofil unserer quadrivalenten und ab der Grippesaison 2025/2026 wieder trivalenten Impfstoffe Influvac und Xanaflu“, kommentierte Simon von Boeselager, Leiter des Deutschlandgeschäfts der Viatris-Gruppe Deutschland. „Wir sind bestrebt, eine zuverlässige Versorgung der Bevölkerung in Deutschland mit unseren Impfstoffen Influvac und Xanaflu zu gewährleisten, und damit dem Zugang zu den trivalenten Impfstoffen für die kommende Grippesaison gerecht zu werden.“
Bildmaterial
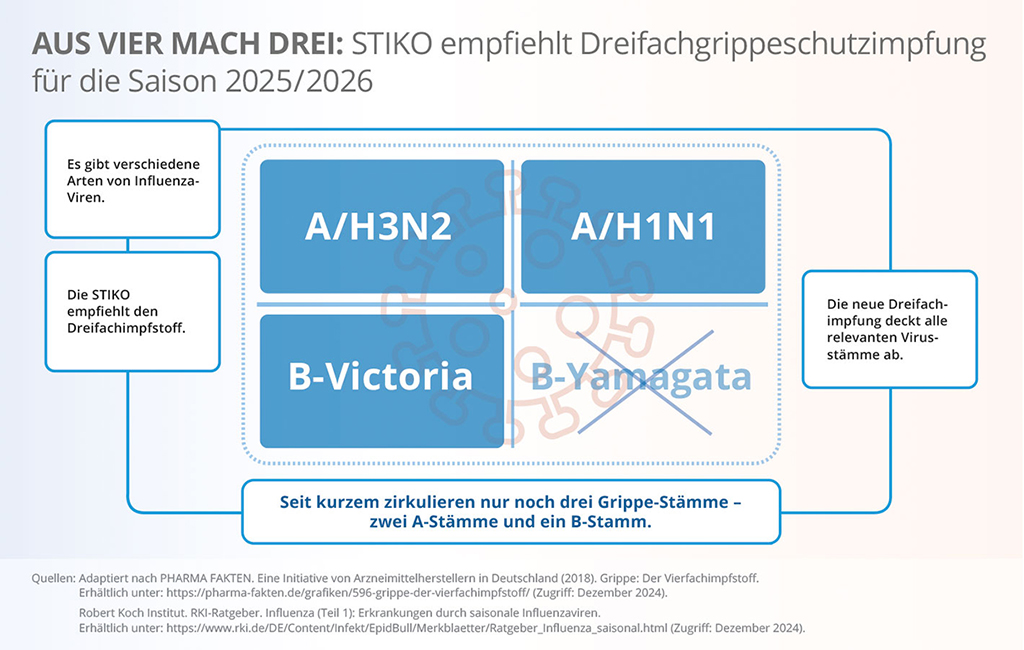
Primäre Abb./Abb. 1: Die Grippeschutzimpfung erfolgte seit der Impfsaison 2018/2019 mit einem quadrivalenten Grippeschutzimpfstoff. Da nun der B/Yamagata-Stamm seit März 2020 nicht mehr in zirkulierenden Influenzastämmen nachgewiesen wurde, empfiehlt die STIKO die Impfung mit einem trivalenten Grippeschutzimpfstoff für die Impfsaison 2025/2026. © Viatris-Gruppe Deutschland
###
Druckfähiges Bildmaterial anbei.
Für Rückfragen und weitere Informationen wenden Sie sich bitte an:
Pressestelle Viatris-Gruppe Deutschland
+49 (0) 6172 – 888 – 1234
Presse-DE@viatris.com
___________________________________________________
1Fachinformation Influvac Saison 2024/2025. Stand: Juli 2024. https://www.fachinfo.de/fi/pdf/025194. Die Zulassung für den trivalenten Influenzaimpfstoff liegt bereits vor, damit dieser in der Saison 2025/2026 zum Einsatz kommen kann.
2Fachinformation Xanaflu Saison 2024/2025. Stand: Juli 2024. https://www.fachinfo.de/fi/pdf/025195. Die Zulassung für den trivalenten Grippeschutzimpfstoff liegt bereits vor, damit dieser in der Saison 2025/2026 zum Einsatz kommen kann.
3Weltgesundheitsorganisation (WHO). Recommended composition of influenza virus vaccines for use in the 2024-2025 northern hemisphere influenza season. Februar 2024. Erhältlich unter: https://www.who.int/publications/m/item/recommended-composition-of-influenza-virus-vaccines-for-use-in-the-2024-2025-northern-hemisphere-influenza-season (Zugriff: Januar 2024).
4European Medicines Agency (EMA). Replacement of quadrivalent seasonal influenza vaccines with trivalent vaccines in the EU. Removal of antigens from B/Yamagata lineage. 18. März 2024. Erhältlich unter: https://www.ema.europa.eu/en/documents/other/replacement-quadrivalent-seasonal-influenza-vaccines-trivalent-vaccines-eu_en.pdf (Zugriff: Januar 2024).
5Robert Koch Institut. Epidemiologisches Bulletin. Aktuelle Daten und Informationen zu Infektionskrankheiten und Public Health. 31/2024.
6Fachinformation Influvac Tetra Saison 2024/2025. Stand: Juni 2024. https://www.fachinfo.de/fi/pdf/024355.
7Fachinformation Xanaflu Tetra Saison 2024/2025. Stand: Juni 2024. https://www.fachinfo.de/fi/pdf/024356.
8European Centre for Disease Prevention and Control (ECDC) (2022). Factsheet about seasonal influenza. 2022. Erhältlich unter: https://www.ecdc.europa.eu/en/seasonal-influenza/facts/factsheet (Zugriff: Januar 2024).
9Nationale Lenkungsgruppe impfen. Influenza – Gemeldete Influenza-Krankheitsfälle in Deutschland, https://www.nali-impfen.de/monitoring-daten/krankheitsfaelle-in-deutschland/influenza/ (Zugriff: Januar 2024).
10Buda S et al. und die AGI-Studiengruppe (2024). ARE-Wochenbericht KW 21/2024. Arbeitsgemeinschaft Influenza – Robert Koch-Institut. doi: 10.25646/12105, https://edoc.rki.de/handle/176904/11668 (Zugriff: Januar 2024).
11De Courville C et al. (Mai 2022). The economic burden of influenza among adults aged 18 to 64: A systematic litera-ture review. Influenza Other Respir Viruses; 16(3):376–385. doi: 10.1111/irv.12963. Epub 5. Febr. 2022.
12Colombo L et al. (2024): Out of focus but still relevant? Influenza-related resource utilization and vaccination cover-age gaps in adults below 60 years of age with underlying conditions: an analysis of 2016–2024 real-world data in Germany. doi: 10.1055/s-0034-1396815, https://www.tandfonline.com/doi/full/10.1080/13696998.2024.2413284 (Zugriff: Januar 2024).
13European Centre for Disease Prevention and Control (ECDC). Seasonal influenza, 2023−2024. Erhältlich unter: https://www.ecdc.europa.eu/sites/default/files/documents/seasonal-influenza-annual-epidemiological-report-2023-2024.pdf (Zugriff: Januar 2024).
14European Centre for Disease Prevention and Control (ECDC) (2024). Systematic review update on the efficacy, effec-tiveness and safety of newer and enhanced seasonal influenza vaccines for the prevention of laboratory confirmed influenza in individuals aged 18 years and over. Stockholm: ECDC.
15Colombo L et al. (Januar–Dezember 2024). Influvac Tetra: clinical experience on safety, efficacy, and immunogenicity. Expert Review of vaccines; 23(1):88–101. doi: 10.1080/14760584.2023.2293241. Epub 15. Dezember 2023.
16Van de Witte SV et al. (2012). Trivalent inactivated subunit influenza vaccine Influvac®: 30-year experience of safety and immunogenicity. Trials in Vaccinology; 1:42–48. doi: 10.1016/j.trivac.2012.10.001.
17Moeller-Arendt M et al. (9. Januar 2023). Enhanced passive safety surveillance of Influvac® and Influvac® Tetra: re-sults from seven consecutive seasons. Vaccine; 41(2):606–613. doi:10.1016/j.vaccine.2022.12.001.
